Accès rapide
Votre carnet de voyageest vide
Mince, votre carnet de voyage est vide !
Utilisez le boutonpour ajouter un lieu ou un événement en favoris !
Matin
Après-midi

Choisir Chambéry Montagnes pour organiser vos congrès, colloques, conventions, séminaires, salons, soirées de gala… c’est bénéficier des nombreux avantages offerts par notre destination.
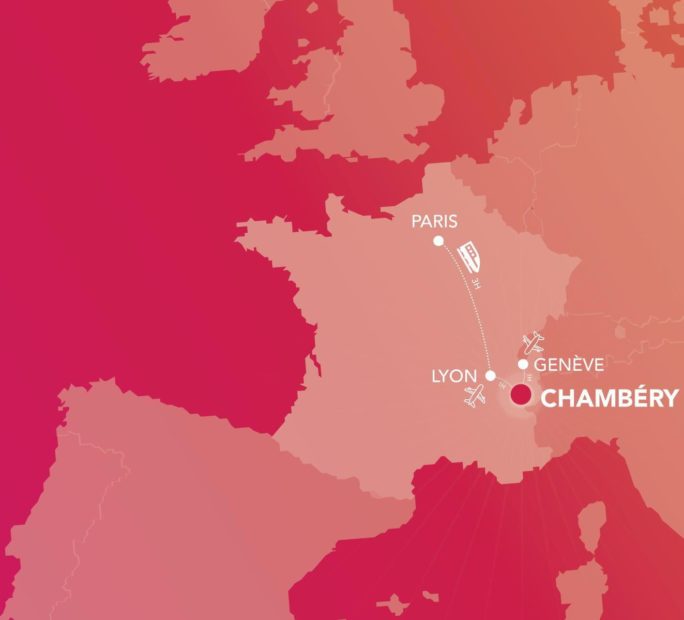
Chambéry Montagnes bénéficie d’une situation géographique privilégiée, au coeur de liaisons alpines qui rendent la destination facilement accessible :
> à moins de 3h de Paris avec 5 à 8 liaisons TGV directes quotidiennes et une gare TGV en centre-ville,
> à 1h de Lyon et Genève par l’autoroute,
> à moins de 45 min de 2 aéroports internationaux (Lyon Saint-Exupéry et Genève Cointrin).

Grâce à la proximité de 3 lacs, dont le plus grand lac naturel de France, de montagnes douces aux paysages authentiques et de vignobles emblématiques des vins de Savoie, vous pourrez monter des programmes complets et variés, dont les activités peuvent se décliner en toute saison, au gré de vos envies : culture, nature, patrimoine, gastronomie, challenge sportif…
Sur terre, sous terre, sur l’eau, dans les airs…les possibilités sont infinies !

> Un parc événementiel entièrement rénové et fonctionnel qui regroupe, sur un même site, deux équipements modulables et complémentaires : un parc des expositions et une salle multifonctionnelle.
> Un centre de congrès idéalement situé en centre-ville. Cet ancien manège de cavalerie datant de l’époque Sarde propose des espaces fonctionnels et chaleureux pour des événements de 100 à 400 personnes.
> Un parc hôtelier de 1400 chambres pour tous les goûts et tous les budgets : une chambre chalet en centre-ville, une chambre dans un château du XVème siècle ou dans une demeure de maître surplombant la ville ou bien encore une suite loft au coeur du centre ancien.
> Des salles de séminaire aux ambiances variées : en centre-ville de Chambéry, dans un aéroport, au cœur des vignobles de Savoie, en montagne, au bord du lac d’Aiguebelette…
> De nombreux lieux réceptifs pour des soirées d’exception

…assuré par des professionnels passionnés, engagés à nos côtés pour vous garantir un service sur-mesure de grande qualité et attachés, comme nous le sommes, aux valeurs d’accueil, de convivialité et d’authenticité qui caractérisent notre territoire et ses partenaires.

Chambéry Montagnes est une destination touristique unique qui offre sur un même territoire :
> Une Ville d’art et d’histoire dont les nombreuses allées, façades médiévales colorées et monuments incontournables comme le Château des Ducs de Savoie témoignent de plus de 1000 ans d’histoire reliant la Savoie et le Piémont.
> Un parc naturel régional labellisé Géoparc à l’Unesco grâce à son patrimoine géologique remarquable, et dont les paysages superbes offrent un bel éventail d’activités dans un cadre exceptionnel… celui du Massif des Bauges.




